
02 Allgemeines zu Batterien und Akkus
Das Thema Energiespeicher in Batterieform ist eine Wissenschaft für sich und sehr umfangreich. Als Roboter-Tüftler ist ein Basiswissen unabdingbar und kann viel Ärger ersparen. Die Energiequelle ist bei Elektronik-Projekten eines der teureren Elemente. Wichtig sind auch die geeigneten Kennwerte der Batterie-Eigenschaften, um den Energiehunger des Gerätes zu decken.
Durch falsche Handhabung und Unkenntnis kann sogar ein nagelneuer Akku unbrauchbar werden. Ein NiMH-Akku hat beispielsweise bei sachgerechtem Gebrauch eine Lebensdauer von ca. 500-1000 Ladezyklen. Die Höhe der Ladezyklen beschreibt, wie oft ein Akku insgesamt aufgeladen werden, bis es unbrauchbar wird. Mit viel Pech kann die Leistung schon durch eine einzige Tiefentladung oder Überladung sich enorm verschlechtern. Sie wäre dann nahezu nutzlos, da sie trotz Vollladung nur kurzzeitig Energie liefert.
Batterie oder Akku?
Ein Dynamo produziert durch mechanische Arbeit elektrischen Strom. Im Gegensatz dazu ist eine Batterie eine Einheit, die durch chemische Prozesse Strom produziert.
Grundsätzlich wird zwischen den primären Batterien (=Primärzelle) und den sekundären Batterien (=Sekundärzelle) unterschieden. Ursprünglich wurden nicht aufladbare Primärzellen als Batterie und wiederaufladbare Sekundärzellen als Akkumulatoren (kurz Akku) bezeichnet. Doch heutzutage werden auch Akkus als (wiederaufladbare) Batterien bezeichnet. Die Primärzelle (Wegwerf-Batterie) erhält bereits bei der Produktion ihre maximale Energie. Die Sekundärzelle oder Akku erhält ihre vollständige Energie erst nach dem Aufladezyklus.

In diesem Tutorial gehen wir nicht weiter auf Primärzellen ein, da sie aus Kostengründen und auf Hinsicht auf die Umwelt für mobile Anwendungen eine eher schlechte Wahl darstellen. Der Gedanke für jede Anwendung einen Akku einzusetzen liegt nahe, doch haben Akkus gegenüber Primärzellen einen entscheidenden Nachteil: Mit der Zeit entladen sich alle Batterien und Akkus durch den sogenannten inneren Ladungsausgleich. Bei Akkus vollzieht sich dieser Prozess durch den internen Aufbau schneller.
Bei Geräten, für die der Batterie-Wechsel selten infrage kommt, setzt man eher auf Primärzellen. Für Geräte, die wenig Strom verbrauchen oder selten benutzt werden, lohnt sich der Einsatz von Akkus durch ihre Selbstentladung eher weniger. Dazu zählen Rauchmelder, Waagen oder Rauchmelder. Die Stromentnahme einer Fernbedienung ist kurz und selten.
Bei Anwendungen mit einem hohen Stromverbrauch und regelmäßigem Gebrauch sind Akkus die bessere Wahl. Dazu zählen z.B. Digitalkameras, Tablets oder Laptops. Es wär ein Unding, in einem Smartphone Wegwerfbatterien einzusetzen.
Aufbau und Funktionsweise eines Akkus
Ein Akku besteht meistens aus mehreren Zellen, deren Kapazität zusammengeführt wird. So besteht z.B. eine ### aus zwei Zellen, deren Strom sich zu 1,2 Volt addieren. So zu sagen sind es mehrere Akkus in einem Gehäuse – es gibt sie auch mit nur einer Zelle.
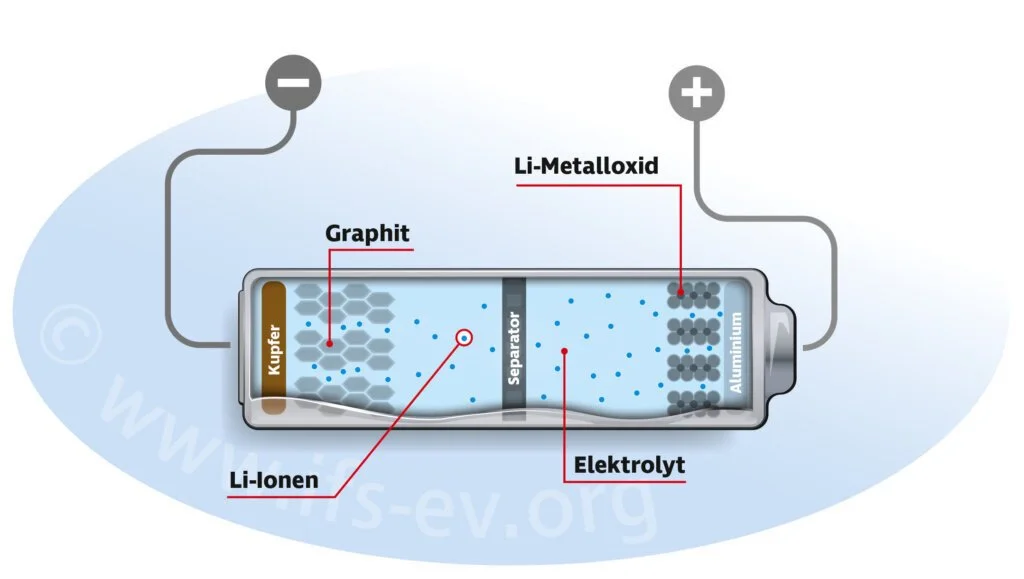
Akkus bestehen aus einer positiven und negativen Elektrode, die in einer Elektrolytlösung platziert sind. Die positive Elektrode wird Anode und die negative Kathode genannt. Beide Elektroden werden durch den Separator getrennt, um Kurzschlüsse zu vermeiden. Der Separator ist so aufgebaut, dass er nur Ionen durchlässt. Unterschiedliche Akkutypen funktionieren mit unterschiedlichen Materialien.
Wird ein Verbraucher an den Akku angeschlossen, passiert folgendes: Zwischen beiden Elektroden baut sich eine Spannung auf. Es finden zwei Strömungen statt: Zum einen der Elektronenfluss von einer Elektrode, durch den Leiter zum Verbraucher und zurück zur Batterie in die andere Elektrode. Und zum anderen findet gleichzeitig innerhalb der Batterie ein Ionenfluss statt. Die Ionen wandern im Elektrolyt von der einen Kammer durch den Separator in die andere Kammer. Sie haben die Aufgabe, die fehlenden Ladungen der Elektronen auf der gegenüberliegenden Elektrode auszugleichen. Auf den genauen chemischen Prozess gehen wir an dieser Stelle nicht ein.
Mit der Zeit entlädt sich der Akku. Der Prozess kommt zum Erliegen, wenn alle Ionen von der einen in die andere Kammer gewandert sind. Bei Akkus ist dieser Entlade-Prozess umkehrbar, in dem man die Batterie wiederaufladet. Der chemische Vorgang des Aufladeprozesses wird Elektrolyse genannt. Die chemischen Reaktionen, die beim Entladen ablaufen, sind nahezu vollständig rückgängig machbar.
Beim Entladen und insbesondere beim Aufladen geht ein Teil der aufgewandten Energie in Form von Wärme verloren. Die Differenz zwischen der benötigten Ladeenergie und der entnehmbaren Energie bezeichnet man als Ladewirkungsgrad. In der Praxis liegt der Wirkungsgrad meistens zwischen 70% und knapp unter 100%, d.h. man muss etwas mehr Ladung in den Akku hineinstecken, als man später entnehmen kann. Der Wirkungsgrad hängt von mehreren Faktoren ab: Akkutyp, Produktionsqualität, dem Einsatz, Umgebungstemperatur, Alter der Akkus oder sogar dem Ladegerät.
Jeder Akkutyp verlangt eine andere Ladetechnik. Es existieren Ladegeräte, die mit verschiedenen Akkus umgehen können. Dank der heutigen integrierten Mikrocontrollersteuerung in den Ladegeräten wird die Batterie über entsprechende Ladeprogramme durch das Messen von Strom, Spannung und Temperatur überwacht und optimal geladen.
Die Akkukapazität
Bei der Auswahl von Akkumulatoren sind Kenntnisse über bestimmte Akkueigenschaften sehr hilfreich. Die Akkukapazität ist eine der meistgebrauchten Kenngrößen. Sie beschreibt das Strom-Fassungsvermögen. Also ein physikalisches Maß für die Strommenge, die in einen Akku reinpassen kann. Sie wird gebildet, in dem man die Stromstärke mit der Zeitdauer multipliziert. Die Einheit wird in Amperestunden (kurz Ah) angegeben. Bei kleineren Akkus wird sie in Milliamperestunden ausgegeben (1A = 1000mAh).
1000 x mA x h ####bild
Von einem vollgeladenem 1000mA Akku kann man einen Strom von 1000mA eine Stunde lang (bis sie entladen ist) entnehmen. Das ergibt die folgende Berechnung: 1000mA x 1h = 1000mAh
Wir könnten auch dem Akku 4 Stunden lang (bis sie entladen ist) einen Strom von 250mA entnehmen und würden auf das gleiche Ergebnis kommen: 250mA x 4h = 1000mAh.
Die Akkuladung
Wenn die Akkukapazität das Fassungsvermögen beschreibt, dann stellt die Ladung die Menge dar. Die Ladung besitzt die gleiche Einheit (Ah). Am besten kann man ein Wasservergleich heranziehen: Ein Wassertank stellt die Akkukapazität dar (maximales Fassungsvermögen) und die Akkuladung gleicht der Wassermenge, die hineingefüllt oder entnommen wurde oder noch im Tank vorhanden ist.
Entnimmt man einem vollgeladenen 1Ah-Akku eine Ladung von 300 mAh (=0,3Ah), besitzt dieser eine Restladung von 800mAh.
####bild
Die Selbstentladung
Die Selbstentladung ist ein unerwünschter Effekt, der bei Sekundärzellen stärker ausgeprägt ist. Der Akku verliert im Laufe der Zeit an Ladung, obwohl kein Verbraucher angeschlossen ist. Ziehen wir noch einmal die Wassermetapher heran: Auch wenn der Wassertank randvoll ist, verdampft täglich ein Teil, obwohl man keinen Tropfen verbraucht hat.
###bild
Natürlich verdampfen keine Elektronen im Akku. Es finden chemische Prozesse statt, die der aktiven Entladung durch einen Verbraucher gleichen.
Die Nennspannung
Die Spannung, die ein Akku liefert, wird Nennspannung genannt. Sie ist der vom Hersteller spezifizierte Wert der elektrischen Spannung und stellt einen Durchschnittswert dar. Die tatsächliche Spannung liegt etwas höher. Beispielsweise hat ein Lithium-Ionen-Akku, mit einer Nennspannung von 3,7Volt, bei voller Ladung in Wirklichkeit eine Spannung von 4,2Volt.
Außerdem ist die angegeben Nennspannung eines Akkus kein konstanter Wert, sondern sinkt während der Entladung. In unserem oberen Beispiel würde die Akkuspannung bei 4,2Volt starten und während des Betriebs bis auf 3,0Volt sinken. Bei 3,0Volt gilt der Akku als entladen. Eine weitere Entladung bedeutet eine Tiefentladung, somit eine Schädigung des Akkus.
Die Tiefentladung
Wird ein Akku so weit belastet, dass die Spannung weit unter die Nennspannung fällt, kommt es zur Tiefentladung. Also das „Auspressen“ eines Akkus bis dieser keinen Strom mehr abgibt, kann innerhalb der Batterie zu irreversiblen Schäden führen. Entweder kommt es zu erheblichen Kapazitätsverlusten oder der Akku wird gänzlich unbrauchbar. Bei dem Beispiel mit dem Lithium-Ionen-Akku ist die Tiefentladung bei 3,0Volt erreicht. Moderne Lithium-Ionen-Akkus besitzen eine interne Elektronik, die den Akku kappt und vor weiterer Entladung schützt.